Bảng tuần hoàn nguyên tố chất hóa học có vai trò vô cùng quan trọng. Nếu những em mong mỏi học xuất sắc môn Hóa, thì cần được “tinh thông” triết lý có vào bảng tuần hoàn. Vậy, phương pháp đọc và phương pháp ghi lưu giữ bảng tuần hoàn hóa học lớp 8, lớp 9, lớp 10 như thế nào? Marathon Education sẽ reviews đến các em tất tần tật về bảng tuần hoàn các nguyên tố chất hóa học qua bài viết sau. Bạn đang xem: Bảng toàn hoàn hóa học

Một số thông tin về bảng tuần trả trong chương trình lớp 10 của Mendeleev:
Khi những nguyên tố mới được kiếm tìm thấy, bảng tuần hoàn cũng trải trải qua nhiều lần điều chỉnh. Tuy nhiên, các vẻ ngoài hiển thị cơ phiên bản vẫn được giữ nguyên như thiết kế ban đầu của Mendeleev. Giá trị chủ đạo mà bảng tuần hoàn nguyên tố hóa học đưa về đó là tài năng phân tích tính chất hóa học tập của một nguyên tố ví dụ dựa vào địa điểm trong bảng. Ngoài việc được áp dụng lúc học Hóa, bảng tuần hoàn cũng rất được sử dụng trong 2 môn Lý và Sinh.Cách xem bảng tuần hoàn hóa học

Cấu tạo ra bảng tuần hoàn những nguyên tố hóa học
Ô nguyên tố: Thể hiện những thông tin về số hiệu nguyên tử, ký hiệu hóa học, thương hiệu nguyên tố, nguyên tử khối của nguyên tố chất hóa học trong ô.Chu kỳ: Dãy những nguyên tố chất hóa học được xếp theo chiều tăng dần đều về điện tích hạt nhân và những nguyên tử của chúng bao gồm cùng số lớp electron. Có tất cả 7 chu kỳ luân hồi trong bảng tuần hoàn nguyên tố hóa học, chu kỳ luân hồi 1, 2, 3 call là chu kỳ nhỏ, chu kỳ 4, 5, 6, 7 call là chu kỳ luân hồi lớn.Nhóm nguyên tố: Tập hợp những nguyên tố có tính chất tương tư nhau vày trong nguyên tử của chúng bao gồm cùng số electron lớp bên ngoài cùng và được xếp thành cột theo chiều tăng ngày một nhiều của năng lượng điện hạt hiền khô dưới lên trên.Chi ngày tiết của một ô nhân tố trong bảng tuần hoàn nguyên tố hóa học
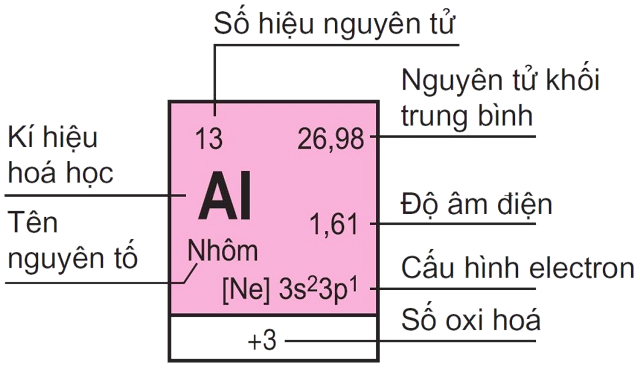
Để vấn đề xem bảng tuần trả hóa những nguyên tố chất hóa học lớp 10 tiện lợi và chuẩn chỉnh xác, các em yêu cầu làm quen với một số trong những thuật ngữ như mặt dưới:
Số hiệu nguyên tử: Còn mang tên gọi không giống là số proton của nguyên tố hóa học. Danh từ bỏ này thể hiện cho số proton của một nguyên tử cùng số năng lượng điện của phân tử nhân. Số hiệu nguyên tử có mức giá trị thông qua số electron trong một nguyên tử trung hòa về điện. Đặc biệt, số hiệu nguyên tử để giúp đỡ xác định nhất một yếu tố hóa học. Nguyên tử khối trung bình: Hầu hết, các nguyên tố hóa học phần lớn là lếu láo hợp của không ít đồng vị khác nhau, bao gồm tỉ lệ tỷ lệ số nguyên tử xác định. Vì chưng đó, nguyên tử khối của các nguyên tố này sẽ được tính bằng nguyên tử khối vừa đủ của tất cả hổn hợp đồng vị dựa theo tỉ lệ xác suất của các nguyên tử tương ứng.Cấu hình electron: Cho thấy sự phân bố của những electron ở phần đa trạng thái năng lượng khác biệt trong lớp vỏ nguyên tử hoặc ở hồ hết nơi mà bọn chúng hiện diện.Độ âm điện: Là kỹ năng hút electron trong quy trình tạo thành link hóa học. Về phần này, những em yêu cầu ghi đừng quên độ âm năng lượng điện tỉ lệ thuận cùng với tính phi kim. Cầm cố thể, giả dụ độ âm năng lượng điện của nhân tố càng lớn, tính phi kim càng táo tợn và ngược lại. Số oxi hóa: Là số sử dụng cho một hoặc 1 đội nguyên tử. Nhờ vào con số này, những em rất có thể tính được số electron điều đình khi thâm nhập phản ứng.Tên nguyên tố: Gồm 1 kiểu dáng nguyên tử duy nhất, được phân biệt dựa trên số hiệu nguyên tử.Ký hiệu hóa học: là tên viết tắt của thành phần hóa học, gồm một hoặc 2 vần âm Latin. Chữ trước tiên thường đang viết hoa.Ancol Isopropylic Là Gì? đặc thù Lý Hóa Và cách làm Ancol Isopropylic
Vị trí của oxi vào bảng tuần trả hóa học

Oxi có cấu hình là 1s22s22p4
Vậy địa chỉ của oxi vào bảng tuần hoàn hóa học là sinh sống ô trang bị 8; chu kỳ 2 (do bao gồm 2 lớp electron); nhóm VIA (do 6 e hóa trị, yếu tắc p)
Ý nghĩa của bảng tuần trả nguyên tố hóa học
1. Lúc biết được địa chỉ của nguyên tố hóa học, ta rất có thể suy ra được đặc điểm và cấu tạo của nguyên tố chất hóa học đó.
Ví dụ: lúc biết nguyên tố X bao gồm số hiệu nguyên tử là 16, thuộc chu kỳ luân hồi 3, nhóm VIA, ta hoàn toàn có thể suy ra được:
Điện tích hạt nhân của yếu tắc X là 16+ và nguyên tố này còn có 16 electron (số hiệu nguyên tử là 16)Nguyên tố X có 3 lớp electron (thuộc chu kỳ luân hồi 3).Lớp kế bên cùng của nhân tố X gồm 6 electron (thuộc nhóm VIA).2. Lúc biết được cấu trúc nguyên tử của yếu tố hóa học, ta rất có thể suy ra được tính chất và vị trí của nguyên tố hóa học kia trong bảng tuần trả nguyên tố hóa học.
Ví dụ: khi biết nguyên tố Y có điện tích phân tử nhân là 12+, gồm 3 lớp electron và lớp bên ngoài cùng bao gồm 2 electron, ta hoàn toàn có thể suy ra được:
Nguyên tố Y nằm ở vị trí ô trang bị 12 (điện tích phân tử nhân là 12+), thuộc chu kỳ luân hồi 3 (có 3 lớp electron), team IIA (lớp quanh đó cùng tất cả 2 electron) trên bảng tuần hoàn.Do nằm tại đầu chu kỳ, đề nghị nguyên tố Y là kim loại.Cách học thuộc cấp tốc bảng tuần hoàn hóa học
Thực tế, bảng tuần hoàn những nguyên tố hóa học 10 có nhiều thông tin. Hãy áp dụng 1 trong những 3 giải pháp sau để vấn đề học thuộc và ghi lưu giữ trở nên đơn giản dễ dàng và hối hả hơn.
Cách 1: phân tích bảng tuần hoàn
Mỗi ô trong bảng tuần hoàn đã hiển thị thông tin về tên, ký hiệu, số hiệu nguyên tử. Chỉ cần ghi nhớ 10 nguyên tố đầu tiên, những em đang tìm ra quy luật cho các nguyên tố còn lại.
Cách 2: In cùng dán bảng tuần trả ở hầu hết nơi dễ nhận ra trong không gian học

Các em hãy dán bảng tuần hoàn ở phần đa nơi dễ dàng quan ngay cạnh và chia thành nhiều phần để học. Điều này thật sự với đến hiệu quả cao trong bài toán ghi nhớ.
Cách 3: Dùng phương pháp để ghi nhớ
Để có thể nhớ lâu kỹ năng trong bảng tuần hoàn, các em cần liên tục làm bài xích tập và áp dụng câu thơ/văn xuôi nhằm ghi nhớ:
Hơn hết, để hoàn toàn có thể nhớ lâu kiến thức và kỹ năng trong bảng tuần hoàn nguyên tố hóa học, những em cần liên tiếp làm bài xích tập và áp dụng câu thơ/văn xuôi nhằm ghi nhớ trăng tròn nguyên tố đầu:
13 Cách cân đối Phương Trình Hóa Học nhanh Và thiết yếu Xác
Hoàng hôn lặn bể Bắc
Chợt nhớ làm việc phương Nam
Nắng mai ánh sương phủ
Song cửa ngõ ai không cài.
| HHoàng | He Hôn | ||||||
| Li Lặng | Be Bể | BBắc | CChợt | NNhớ | OỞ | FPhương | Ne Nam |
| Na Nắng | Mg Mai | AlÁnh | Si Sương | PPhủ | SSong | Cl Cửa | Ar Ai |
| KKhông | Ca Cài |
Hoặc một số câu nói học tập thuộc như: “khi nào bắt buộc may áo gần cạnh sắt ghi nhớ sang phố hỏi cửa hàng Á Phi Âu” khớp ứng cho F, Na, Ca, Mg, Al, Zn, Fe, Ni, Sn, Pb, H, Cu, Hg, Ag, Pt, Au. “Lâu nay không thư thả coi phim” khớp ứng với Li, Na, K, Rb, Cs, Pr.
Cách 4: bài xích ca hóa trị
Áp dụng bài bác ca hóa trị để học ở trong bảng tuần hoàn những nguyên tố hóa học:
“Kali, I – ốt, Hidro
Natri cùng với Bạc, Clo một loài
Là hóa trị 1 bạn ơi
Nhớ ghi mang lại rõ kẻo rồi phân vân
Magie, Chì, Kẽm, Thủy ngân
Canxi, Đồng ấy cũng gần Bải
Cuối cùng thêm chú Oxi
Hóa trị 2 ấy bao gồm gì khó khăn khăn
Bác Nhôm hóa trị 3 lần
Ghi sâu đầu óc khi cần có ngay
Cacbon, Silic này đây
Là hóa trị 4 ko ngày làm sao quên
Sắt kia đề cập cũng thân quen tên
2, 3 tăng và giảm thật phiền lắm thôi
Nito rắc rối nhất đời
1, 2, 3, 4 khi thời sản phẩm công nghệ 5
Lưu huỳnh lắm lúc chơi khăm
Xuống 2, lên 51 lúc nằm trang bị 4
Photpho nói tới không dư
Nếu ai hỏi mang lại thì hừ rằng 5
Em ơi nỗ lực học chăm
Bài ca hóa trị trong cả năm rất cần”.
Bảng tuần hoàn hóa học rõ nét, khá đầy đủ nhất
Để giúp các em rất có thể học tập hiệu quả, Marathon Education vẫn tổng hợp các file pdf, file ảnh bảng tuần hoàn chất hóa học rõ nét, không hề thiếu nhất lớp 8, lớp 9, lớp 10 dưới đây. Các em rất có thể tải bảng tuần hoàn chất hóa học về nhằm học tập với ghi nhớ:

Bài tập áp dụng có đáp án
Bài tập SGK Hóa 9
Bài 1 Trang 101 SGK Hóa 9Nêu kết cấu nguyên tử, đặc thù kim loại và đặc thù phi kim của các nguyên tố tất cả số hiệu nguyên tử theo thứ tự là 7, 12, 16.
Lời giải:
Gọi A, B, C là 3 nguyên tố gồm số hiệu nguyên tử theo yêu ước đề bài, dựa vào bảng thành phần hóa học, ta gồm bảng sau:
| Nguyên tố | Số hiệu nguyên tử | Cấu chế tạo nguyên tử | Tính chất | ||||
| Điện tích phân tử nhân | Số e vào nguyên tử | Số lớp electron | Số e lớp bên ngoài cùng | Kim loại | Phi kim | ||
| A | 7 | 7+ | 7 | 2 | 5 | x | |
| B | 12 | 12+ | 12 | 3 | 2 | x | |
| C | 16 | 6+ | 6 | 3 | 6 | x |
Cho biết nguyên tố X có cấu trúc nguyên tử với năng lượng điện hạt nhân là 11+, 3 lớp electron, lớp ngoài cùng có một electron. Xác định vị trí của thành phần X trong bảng tuần hoàn.
Lời giải:
Vị trí của nhân tố X vào bảng tuần hoàn:
Ô số 11 (điện tích phân tử nhân là 11+)Chu kì 3 (3 lớp electron)Nhóm I (lớp bên cạnh cùng có 1 electron)Từ 3 thông tin trên, ta hoàn toàn có thể kết luận:
Tên yếu tố X là Natri.Ký hiệu chất hóa học là Na.Nguyên tử khối là 23.Bài 3 Trang 101 SGK Hóa 9Đặc điểm của những nguyên tố thuộc team I mọi là những kim loại mạnh tựa như Natri (có khả năng tác dụng với nước tạo nên thành dung dịch kiềm hóa giải khí hidro, chức năng với oxi tạo nên thành oxit, công dụng với phi kim khác tạo ra thành muối). Hãy viết 3 phương trình làm phản ứng minh họa cùng với Kali.
Lời giải:
Kali công dụng với nước sản xuất dung dịch kiềm cùng giải phóng khí hidro.2K + 2H2O → 2KOH + H2
Kali chức năng với oxi chế tác thành oxit.Xem thêm: Top 10 Phòng Tập Gym Linh Đàm
4K + O2 → 2K2O
Kali công dụng với phi kim tạo thành muối.2K + Cl2 → 2KCl
Bài 4 Trang 101 SGK Hóa 9Đặc điểm của các nguyên tố thuốc nhóm VII phần lớn là số đông phi kim mạnh tương tự Clo (trừ At) (có khả năng tính năng với số đông kim nhiều loại tạo thành muối, chức năng với hidro chế tạo ra thành hợp chất khí). Hãy viết 3 phương trình bội nghịch ứng minh hoạ cùng với Brom.
Lời giải:
Brom tác dụng với kim loại tạo thành muối.Br2 + 2K → 2KBr
3Br2 + 2Fe → 2Fe
Br3
Br2 + H2 → 2HBr (k)
Bài 5 Trang 101 SGK Hóa 9Hãy cho thấy cách bố trí nào dưới đây đúng theo chiều tính kim loại giảm dần và lý giải sự lựa chọn:
a. Na, Mg, Al, K
b. K, Na, Mg, Al
c. Al, K, Na, Mg
d. Mg, K, Al, Na
Lời giải:
b là lời giải đúng vì
Các nguyên tố Na, Mg, Al ở thuộc chu kì, theo chiều tăng nhiều điện tích phân tử nhân, tính sắt kẽm kim loại giảm.Các yếu tắc Na, K ở cùng một nhóm, theo chiều tăng điện tích hạt nhân, tính sắt kẽm kim loại tăng.Bài tập SGK Hóa 10
Bài 1 Trang 35 SGK Hóa 10Các yếu tố xếp ngơi nghỉ chu kì 6 gồm số lớp electron vào nguyên tử là:
a. 3
b. 5
c. 6
d. 7
Lời giải:
c là câu trả lời đúng.
Bài 2 Trang 35 SGK Hóa 10Trong bảng tuần hoàn các nguyên tố, số chu kì nhỏ và số chu kì khủng là:
a. 3 với 3
b. 3 với 4
c. 4 với 4
d. 4 và 3
Lời giải:
b là lời giải đúng.
Bài 3 Trang 35 SGK Hóa 10Số yếu tố trong chu kì 3 cùng 5 là:
A. 8 cùng 18
B. 18 cùng 8
C. 8 với 8
D. 18 và 18
Lời giải:
a là giải đáp đúng.
Bài 4 Trang 35 SGK Hóa 10Trong bảng tuần hoàn, các nguyên tố được thu xếp theo bề ngoài nào?
a. Theo chiều tăng của điện tích hạt nhân
b. Những nguyên tố gồm cùng số lớp electron vào nguyên tử được xếp thành 1 hàng
c. Các nguyên tố gồm cùng số electron hóa trị trong nguyên tử được xếp thành 1 cột
d. Cả A, B, C
Lời giải:
d là câu trả lời đúng.
Bài 5 Trang 35 SGK Hóa 10Tìm câu sai trong số câu sau đây:
a. Bảng tuần hoàn có có những ô nguyên tố, những chu kì và những nhóm.
b. Chu kì là dãy các nguyên tố mà nguyên tử của chúng gồm cùng số lớp electron, được thu xếp theo chiều năng lượng điện hạt dìm tăng dần.
c. Bảng tuần hoàn gồm 7 chu kì. Số sản phẩm công nghệ tự của chu kì thông qua số phân lớp electron trong nguyên tử.
d. Bảng tuần hoàn gồm 8 team A cùng 8 team B.
Lời giải:
c là câu trả lời đúng.
Câu đúng: Bảng tuần hoàn có 7 chu kì. Số trang bị tự của chu kì thông qua số lớp electron trong nguyên tử.
Bảng tuần hoàn chất hóa học 10 không hề lạ lẫm với chúng ta học môn hóa trong lịch trình trung học cửa hàng hay trung học càng nhiều nữa. Mặc dù để bạn học giỏi và nhớ thọ phải cần đến phương thức học hay. Con kiến Guru trình làng đến chúng ta học sinh một số mẹo ghi nhớ giỏi bảng tuần hoàn hóa học 10.
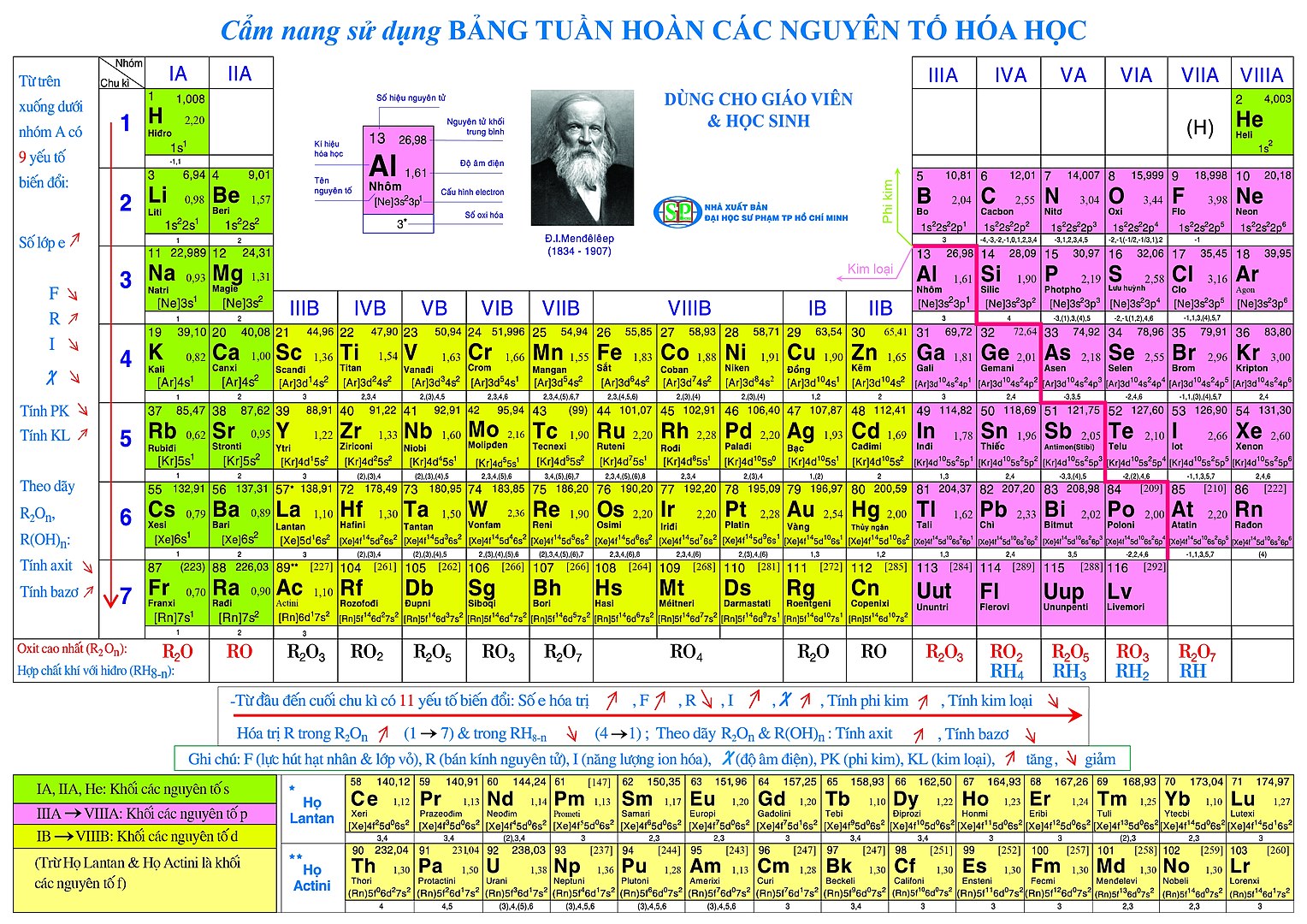



III. Cách ghi ghi nhớ bảng tuần hoàn chất hóa học 10
Sau đó là 2 giải pháp giúp các bạn học sinh ghi nhớ xuất sắc bảng tuần hoàn chất hóa học 10.
1. Nghiên cứu và phân tích bảng tuần hoàn chất hóa học 10
Xác định bản chất các thành phần khác biệt của từng nguyên tố hóc học. Vào bảng tuần hoàn hóa học 10, mỗi một ô sẽ bao gồm nguyên tố gồm các thuộc tính, yếu tố của yếu tố đó. Bởi vì thế, để khám phá bảng tuần hoàn, bạn nên biết tên yếu tắc cùng ký hiệu hóa học, số nguyên tử… toàn bộ các tin tức này đều có trong ô yếu tố đó.
Ghi nhớ cùng thành thành thạo 10 nguyên tố đầu tiên trong bảng, bạn sẽ tìm ra quy luật cho những giá trị nguyên tố tiếp theo. Sau đó, các bạn sử dụng cách thức so sánh với cái giá trị đang học. Cứ như vậy, các bạn sẽ học không còn hơn 120 nguyên tố trong bảng tuần trả Mendeleev.
2. In bảng tuần hoàn hóa học 10 ra một bản màu dán nhằm trong cặp
Bạn hoàn toàn có thể in hoặc tải một bảng tuần hoàn, bạn sẽ mang đi khắp nơi và học bất cứ khi nào thuận tiện. Hãy in thiệt nhiều bản và dán đông đảo nơi cần thiết trong không gian học. Hãy ghim một tờ lưu ý trên bạn dạng dán đôi lúc bạn phải ghi nhớ. Hoặc hoàn toàn có thể chụp lại bạn dạng chính và để ở nơi các bạn dễ quan lại sát. Thường xuyên xuất hiện thêm xem để nhớ được lâu hơn. Có thể tạo thành các phần nhỏ tuổi để học thay do nhồi nhét vô số nguyên tố.
3. Dùng phương thức ghi ghi nhớ bảng tuần hoàn hóa học 10
Dùng cách thức ghi đừng quên viết một vài cụm từ, một vài ba câu giúp đỡ bạn nhớ cấp tốc hơn trong số nguyên tố hóa học. Phương pháp nhớ cấp tốc và nhiều năm nhất là liên tục làm bài bác tập hóa học cùng tra bảng tuần trả hóa học.
Cách nhớ hàng kim loại dễ ợt nhất: K mãng cầu Ca Mg Al Zn sắt Ni Sn Pb H Cu Hg Ag Pt Au – lúc nào cần may áo gần cạnh sắt lưu giữ sang phố hỏi siêu thị áo phi âu.
Kiến Guru sẽ gửi tới các bạn một số cách thức giúp ghi nhớ thọ bảng tuần hoàn chất hóa học 10. Mặc dù nhiên, giải pháp làm nhanh giúp bạn trở thành một người xuất sắc hóa đích thực là tiếp tục giải những bài tập về hóa học, tra với xem những nguyên tố hóa học. Tiến hành các phương pháp cân bằng hòa học cần thiết.














